研究内容
有機反応は、人工的にデザインされた分子の合成に多用される一方、生体内を含むあらゆる環境において恒常的に行われている自然の営みでもあります。我々のグループは有機反応化学の深化と応用を基盤とし、創薬、医学、生命科学研究を革新する分子の創製に取り組むとともに、生体機能の可視化および制御に資する新たな方法論を創出します。
参考動画
2023年3月3日にオンラインで開催された
第15回ABC-InFO講演会で丹羽が発表しました。
1)全く新しい変換を実現する有機反応化学
現時点では不可能とされる化学変換を、新反応の開発により実現します。新たに見いだした反応のメカニズムを追求し、さらに一般化させることで、理学としての有機反応化学を深めます。
生物活性化合物を迅速に機能化する分子リノベーション技術
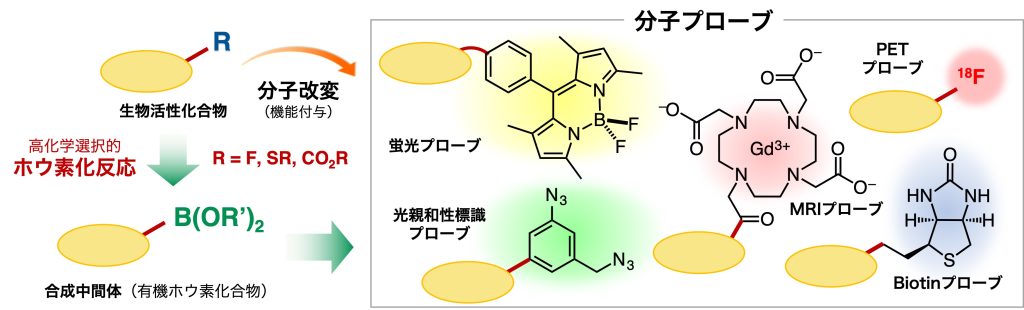
創薬や生命科学研究において、生物活性化合物の機序解明は重要な課題です。そのための一つの手法として、もとの分子を改変して機能化した分子プローブの利活用がありますが、一般にそれらの合成には多大な労力がかかります。これは生物活性化合物がもともと複雑な化学構造を持つことに加え、改変位置によっては元の化合物の合成法を踏襲できず、合成ルートの再開拓を求められることなどによります。
これに対し、研究対象の生物活性化合物そのものを位置選択的にホウ素化し、生じた炭素–ホウ素結合を変換すれば、原理的にわずか2つの工程で、任意の機能を有する分子プローブが得られると着想しました1。
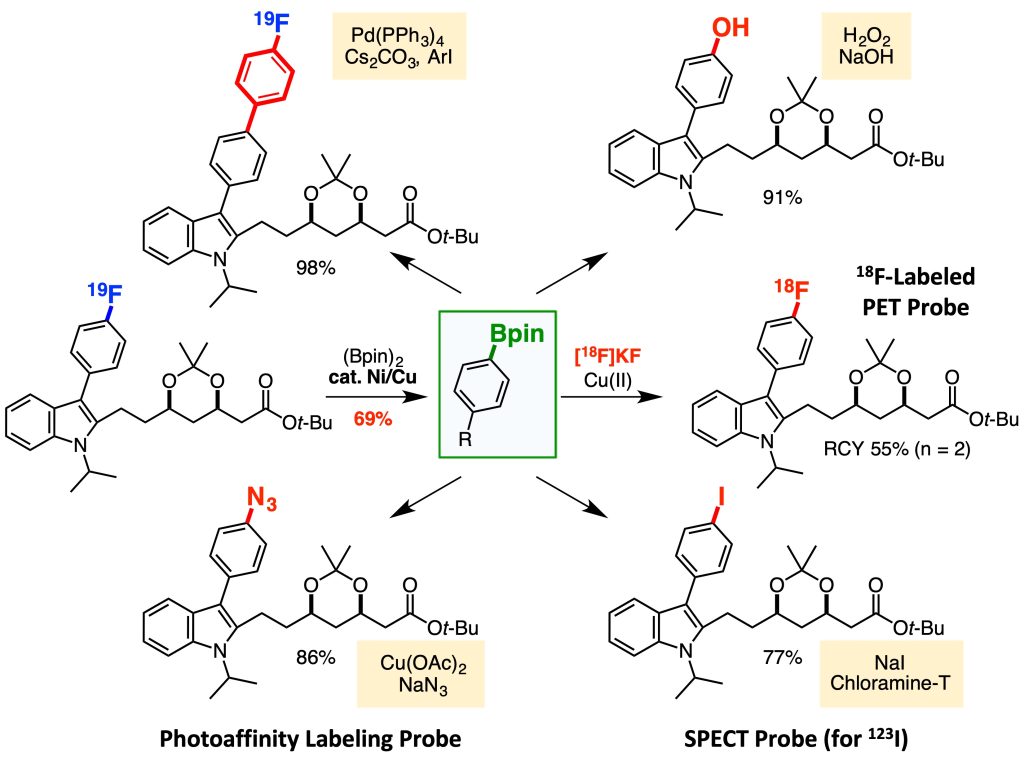
この発想の元、医薬品に広く見られる芳香族フッ化物に着目し、炭素–フッ素結合の切断を経るホウ素化反応を開発しました2-4。この反応は、最も安定な(反応性の低い)炭素–フッ素結合を一定の反応性を示す炭素–ホウ素結合へと変換する、いわば矛盾をはらんだ化学変換ですが、ニッケル錯体や銅錯体を触媒として用いることで進行することを明らかにしました。実際にこの技術を用いて、高脂血症治療薬であるスタチン誘導体を、わずか二段階で18F-標識PETプローブへと作り変えることに成功しました。
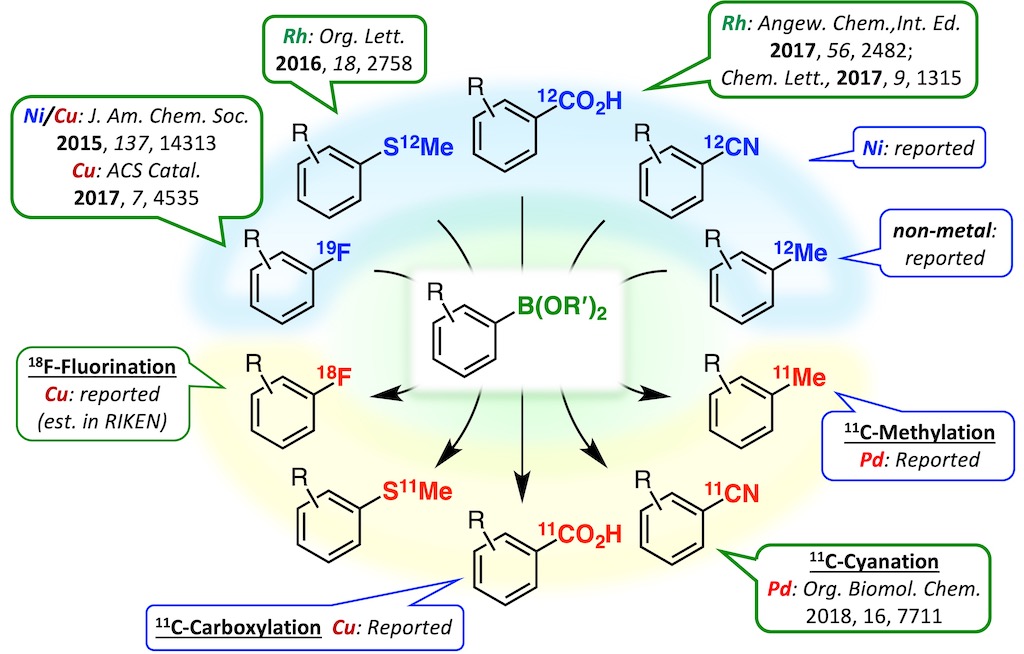
この結果を受け、様々な官能基をボリル基に変換する手法の開発を進めました5-7。この技術をさらに拡張することで、生物活性化合物の分子プローブ化を大幅に簡便化かつ加速し、学際領域の研究の進展を促します。
1. Review: Bull. Chem. Soc. Jpn. 2020, 93, 230–248.
2. J. Am. Chem. Soc. 2015, 137, 14313–14318.
3. ACS Catal. 2017, 7, 4535–4541.
4. Review: 有機合成化学協会誌 2019, 77, 883–894.
5. Org. Lett. 2016, 18, 2758–2761.
6. Angew. Chem., Int. Ed. 2017, 56, 2482–2486.
7. Chem. Lett. 2017, 46, 1315–1318.
2)多様な外部刺激を駆使した精密改変技術
化学変換は共有結合の切断を伴うため、大きなエネルギーを持つ反応性化学種を必要とします。しかし、機能性分子のような複雑化合物に反応性化学種を作用させると、望まぬ位置での化学反応(副反応)が頻発します。そこで多彩な外部刺激を用いて、反応性化学種をゆっくり発生させることで、望みの位置のやさしい変換を実現します。
ルイス酸を用いる鈴木・宮浦クロスカップリング反応
鈴木・宮浦クロスカップリング反応は、信頼性の高い炭素–炭素結合形成法の一つです。この反応では、有機ホウ素化合物の求核性を向上させ金属交換を進行させるために、塩基の添加を必要とします。一方、塩基性条件で競争的に進行する有機ホウ素化合物の脱ホウ素プロトン化による効率低下が課題として知られています。実際、その構造によっては全くカップリング生成物が得られない例もあります。
この課題を解決する単純な戦略として、塩基を使わない新たな反応条件の開拓があります。実際、高い反応性を持つアリールジアゾニウム塩をカップリング剤として用いた場合、塩基を添加せずとも反応が進行することが知られています。しかし、中間体として生じるパラジウムカチオン性錯体が熱的に不安定であるためか、一般的にクロスカップリング反応に用いられる芳香族ハロゲン化物などは適用できません。
このような状況の中、我々は偶然にも、一部のルイス酸の添加が芳香族ハロゲン化物を用いる鈴木・宮浦クロスカップリング反応を進行させることを見いだしました1。温度可変NMRや計算化学などによる解析のほか、共同研究を通じた放射光施設でのXAS測定を用いて詳細に検討した結果、パラジウムと亜鉛の両方の原子を持つカチオン性二核錯体が、比較的安定な中間体として存在することが示唆されました。さらなる検証の結果、この錯体から徐々に亜鉛部位が乖離することで、高反応性のカチオン性錯体をゆっくり発生させていると推察されました。これが加熱条件に耐え、芳香族ハロゲン化物の利用が可能になった理由だと考えています。現在は、この「反応性化学種をゆっくり発生させる」新たな機構を駆使した化学変換の開発に取り組んでいます。
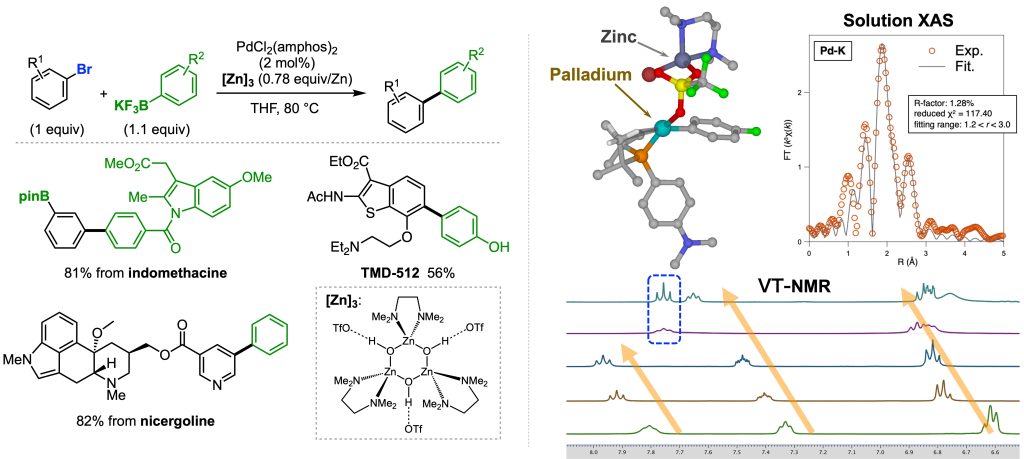
1. Nat. Catal. 2021, 4, 1080–1088.
3)創薬、医学、生命科学分野の発展に資する機能性分子の創出
機能を持つ分子は薬学、医学や生命科学など様々な領域で求められます。しかし、その設計や合成は容易ではありません。周辺分野の研究者との共同研究を通じ、真に求められる機能性分子を、独自の、あるいは最先端の有機反応を駆使して効率的に創出します。
分子プローブの開発
これまでに多数の異分野の研究者と共同して、様々な分子プローブの開発に関わってきました。特に、陽電子放射断層撮像(PET)に用いるPETプローブをこれまでに多数開発してきました。PETイメージングは分子の生体内での局在を動的、立体的、定量的に可視化でき、ヒトにも適用できる稀有な技術です。我々はPETイメージングを活用した創薬、生命科学、医学研究の推進のために、様々な研究背景に応じて、生物活性化合物の探索、寿命の短いPET核種(例えば炭素11の半減期は20.4分、フッ素18の半減期は109.8分)を導入するための標識反応の開発、さらに複雑な化学構造へのPET核種の導入(合成)戦略の立案と実施まで一貫して取り組んできました。これからも共同研究者の多様なニーズに合わせ、様々な機能性分子プローブを積極的に開発していきます。
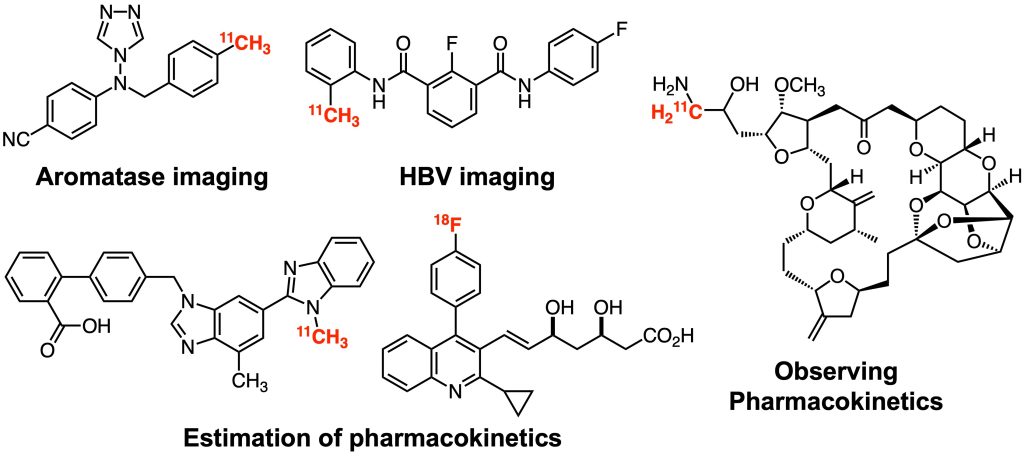
1. Org. Biomol. Chem. 2018, 16, 7711–7716.
2. Mol. Pharmaceutics 2020, 17, 1884–1898.
3. J. Neurosci. Res. 2020, 98, 2208–2218.
4. Drug Metab. Pharmacokinet. 2022, 44, 100449.
5. Bull. Chem. Soc. Jpn. 2023, 96, 283–290.
6. Compr. Psychiatry 2023, 123, 152381.
7. Angew. Chem. Int. Ed. 2023, 62, e202302956.